在生物医药产业飞速发展、药品安全管控日趋严格的当下,鲎试剂作为药品、生物制品、医疗器械细菌内毒素检测的核心试剂,是保障医疗用药安全不可或缺的关键产品,其质量与规范性意义非凡。而早期由中华人民共和国卫生部颁发的部标准WS1-364(B-123)-91,显然不能满足鲎试剂的多元化应用和快速发展的需要。为此需要迫切建立多方法学且有针对性统一的鲎试剂标准。

我司厦门鲎生科积极深度参与《药品检验检测机构 凝胶检测技术鲎试剂质量标准》T/CNPHARS0002-2025、《药品检验检测机构 光度检测技术鲎试剂质量标准》T/CNPHARS0003-2025的鲎试剂团体标准制定工作,更新完善凝胶检测技术鲎试剂的质量指标,同时填补了光度法检测技术鲎试剂在行业的空白,以自身技术积淀与实践经验,促进行业发展新规范。

厦门鲎生科作为鲎试剂内毒素检测行业深耕多年的企业,凭借在行业内48年的技术积累和实践经验及大量实验数据,梳理行业核心需求、整合前沿技术经验,在团体标准修订过程中提出多项建设性、可落地的技术建议,并被正式采纳,包括:
1、优化关键术语定义
2、明确产品鉴别方式及指标
3、细化检测限验证方式及要求
特别是标准中关于检测限项目的标准,我司建议了反应时间差异的高要求,阴性对照与曲线最低点反应时间的区分度反应鲎试剂的对于微量内毒素的灵敏度及识别度,应有一定的反应时间区别。
中华人民共和国卫生部《鲎试剂》WS1-364(B-123)-91中鉴别有三项目,但并不是各个方法学鲎试剂鉴别的专属项,对此我司建议根据不同方法学建立不同的具有专属性的鉴别方式及其指标。这些改进显著提升了相关标准的科学性、严谨性与可操作性,为行业应用提供了更清晰、更可靠的技术依据。


参与标准制定,考验的是企业技术硬实力,而践行标准要求,彰显的是企业的责任与担当。标准的生命力在于落地,而产品则是标准落地的最佳载体。我司产品技术指标:
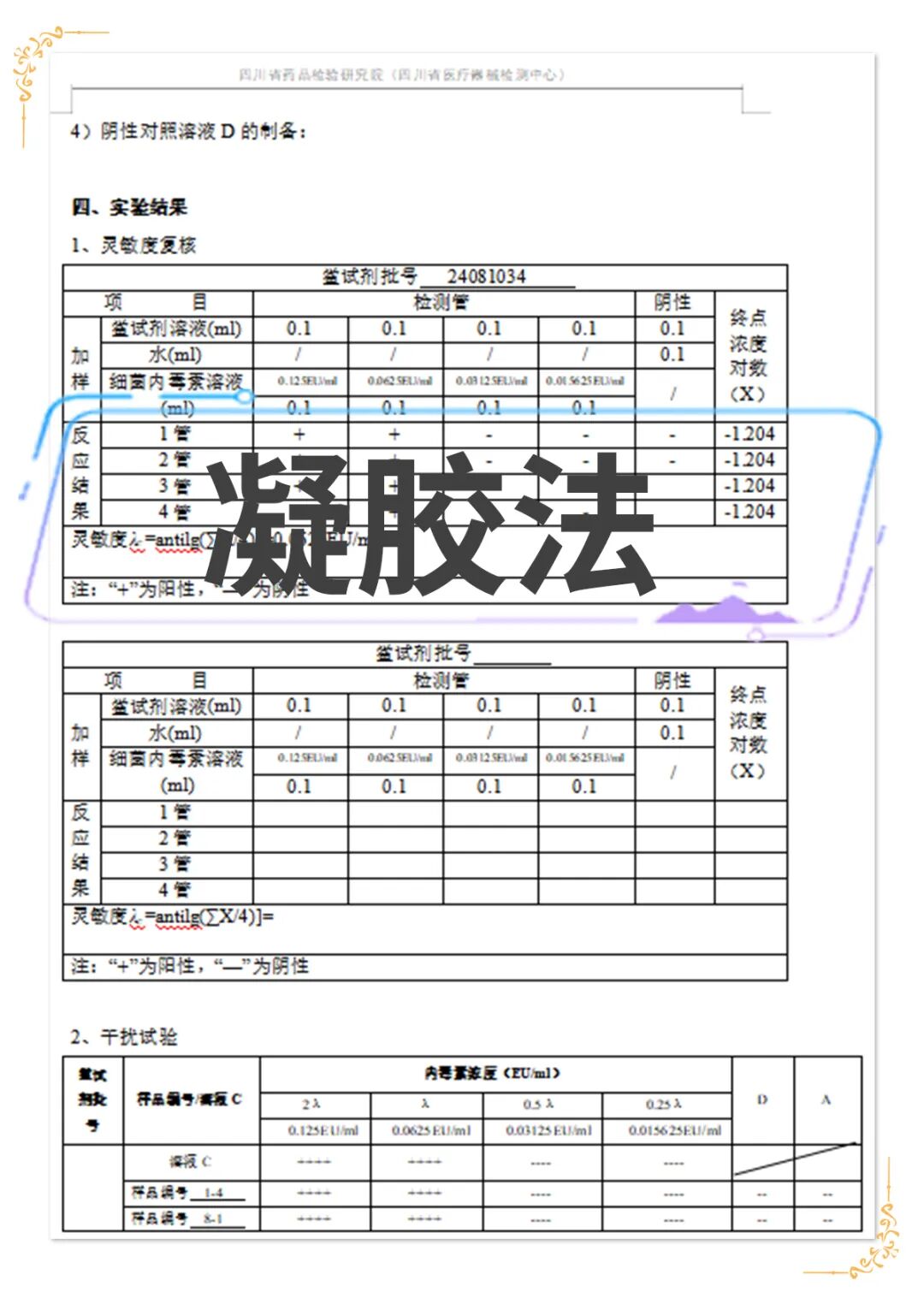
凝胶法鲎试剂
1、灵敏度范围:0.03 EU/mL–1.0 EU/mL
2、批内精密度:CV≤15%
3、水分含量、缓冲能力、自身凝集等关键质控指标均达到或优于标准要求
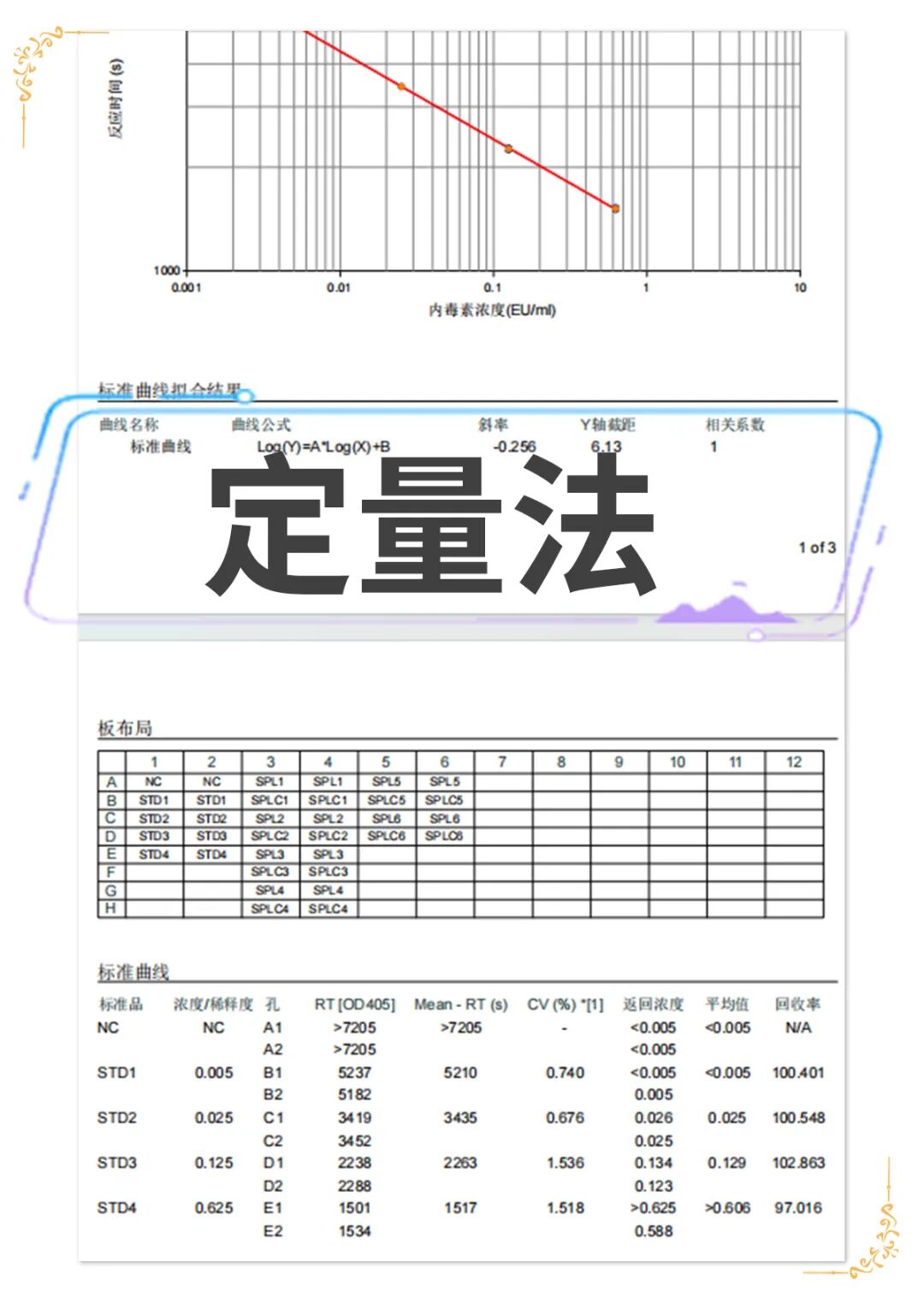
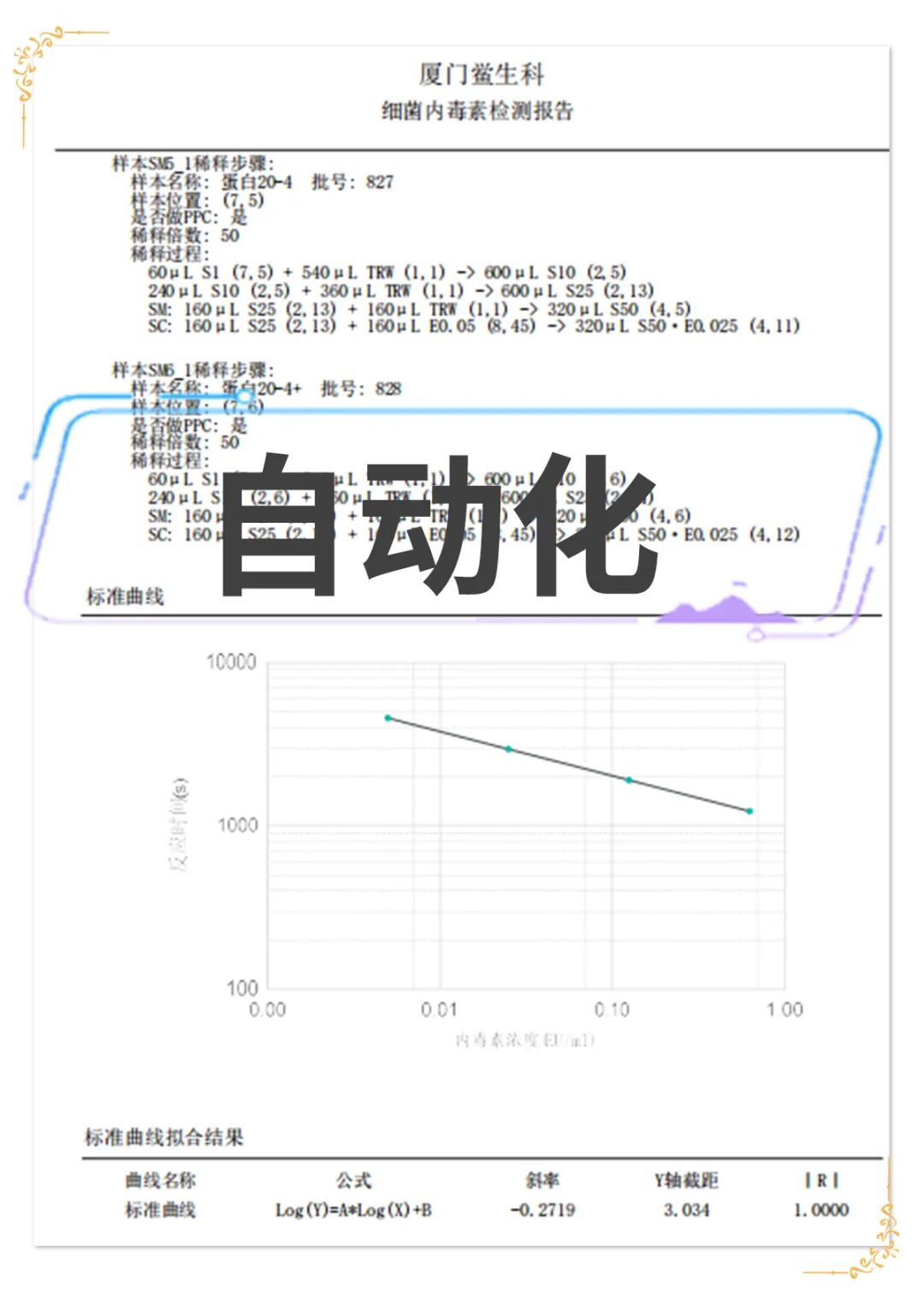
光度法鲎试剂
1、检测限范围:0.001-10EU/mL
2、标准曲线相关系数:│r│≥0.980
3、批内精密度:CV≤10%
4、水分含量、缓冲能力等关键质控指标均达到或优于标准要求
5、准确度回收率稳定在 50%–200%,数据可靠性突出。

除了产品本身的优势,我司还依托标准要求,完善的产品的服务体系。建立“产品+服务”双标准化的模式,从产品咨询、技术支持、售后服务为客户提供一站式、标准化的服务,解决客户的各种疑难杂症。


